Introduction à la mécanique quantique :
Ce thème sur les transferts d'énergie au niveau microscopique est une première approche d'une mécanique nouvelle, la mécanique quantique, qui a commencé à se dessiner au début du XXème siècle, avec notamment la nécessité de comprendre les spectres d'émission ou d'absorption atomique, comme ceux représentés ci-dessous :
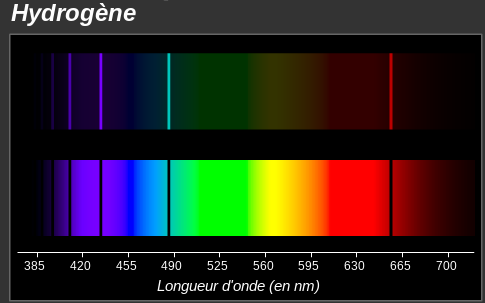
source : ostralo.net
Les pages qui suivent dans les onglets ci-dessous ne déroulent pas l'historique des découvertes mais en présentent les résultats que tout lycéen doit connaître avant la fin de son cursus scolaire.
Le prolongement naturel de ces découvertes amènent à celle du laser et de ses applications si nombreuses aujourd'hui, mais aussi à cette notion étrange de dualité onde-particule, l'un des fondements de la mécanique quantique.
Transitions spontanées
I- Emission et absorption spontanées
A- Niveaux d'énergie dans un atome :
Pour expliquer le fait qu'un atome ne peut émettre ou absorber que des raies de lumière (donc des longueurs d'onde) bien particulières, on a donné à l'atome une structure énergétique en couches :
un atome ne peut exister que dans certains niveaux d'énergie :
on dit que l'énergie du noyau est quantifiée :
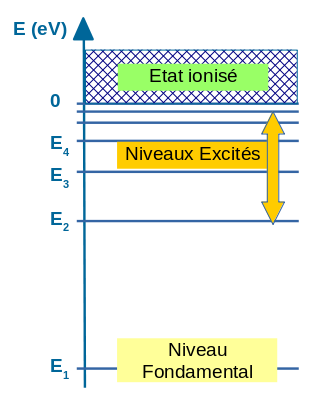
Le niveau le plus bas, est appelé niveau fondamental : c'est dans ce niveau d'énergie que l'on trouve la plupart du temps l'atome. L'atome est alors dans son état "normal".
Les autres niveaux (d'énergie supérieure) sont appelés niveaux excités.
On remarque que ces diagrammes énergétiques sont gradués en eV (électron-volt) et que tous les niveaux d'énergie possibles pour l'atome sont en dessous de la valeur 0, donc négatifs
Ces niveaux d'énergie sont liés à la structure électronique de l'atome et portent donc aussi le nom de "niveaux électroniques".
Par exemple, l'atome d'hydrogène qui n'a qu'un seul électron a une structure électronique notée (K)1 : l'électron est dans le niveau électronique K . L'atome d'hydrogène est alors dans son état fondamental, pour lequel l'énergie vaut E1. Il peut arriver (on verra comment après) que l'atome d'hydrogène reçoive assez d'énergie pour passer au niveau E2 : ceci correspond à une transition électronique, l'électron de l'atome d'hydrogène étant passé du niveau K au niveau L :
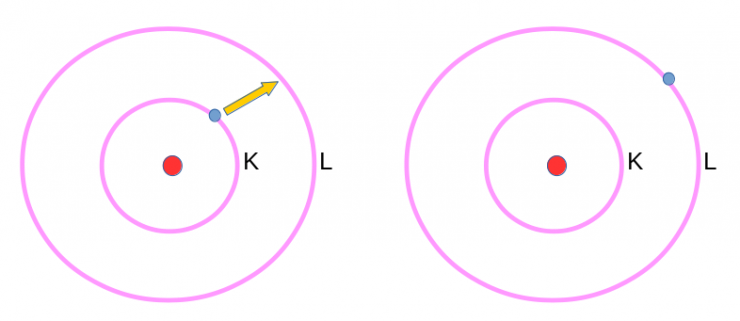
électron lié à l'atome d'hydrogène :
- au niveau fondamental
- au premier niveau excité
Plus l'apport d'énergie est important et plus l'électron passe sur un niveau électronique éloigné du noyau. Pour un apport d'énergie suffisant, l'électron n'est plus lié à l'atome et le quitte : l'atome est devenu un ion ; il est dans un état ionisé. Cette énergie nécessaire pour passer de l'état fondamental à l'état ionisé est appelée énergie d'ionisation : Ei.
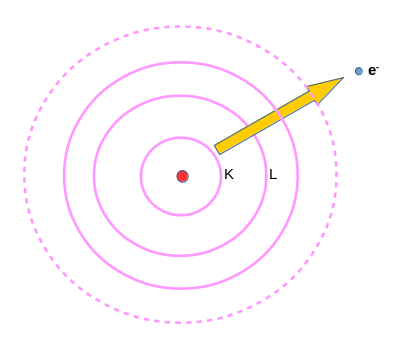
électron non lié : à la place de l'atome H, c'est l'ion H+
L'énergie d'ionisation, c'est l'énergie nécessaire pour faire passer
l'atome de la valeur d'énergie E1 à la valeur 0 eV.
On a donc :
Ei = 0 - E1
Remarque : les états excités sont des états pour lesquels le niveau d'énergie de l'atome est supérieur à celui du niveau fondamental, ces états excités sont donc obtenus lorsque l'atome reçoit (et capture) de l'énergie provenant de l'extérieur.
Cette énergie peut provenir par exemple de décharges électriques ( = chocs d'électrons à grande vitesse) comme on le fait dans les lampes spectrales.
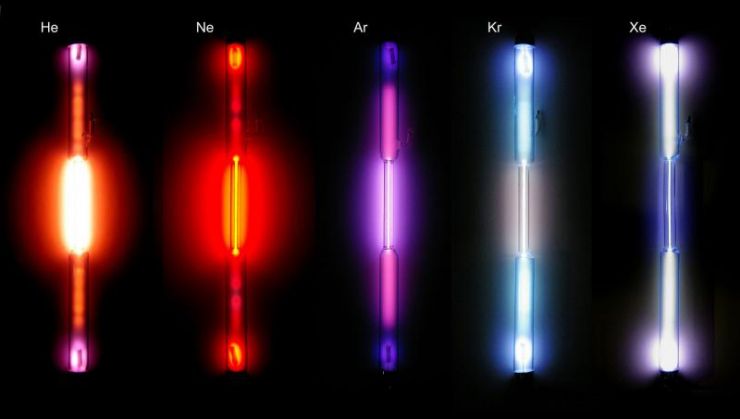
Différentes lampes spectrales : hélium, néon, argon, krypton, xénon
source : sonodis.fr
... Mais on verra aussi que cette énergie d'excitation peut provenir d'une radiation lumineuse (paragraphe C)
B- Emission de lumière par un atome :
1- Désexcitation d'un atome :
On se place dans le cas où un atome se trouve dans un niveau excité (suite par exemple à une décharge électrique).
L'atome ne reste que très peu de temps dans un état excité : il "retombe" vers son niveau fondamental :
- directement
- ou éventuellement en passant par des niveaux intermédiaires s'il y en a.
On dit que l'atome se désexcite.
Ainsi, si un atome est dans le niveau E4, pour retourner au niveau fondamental E1, plusieurs voies de désexcitation sont possibles :
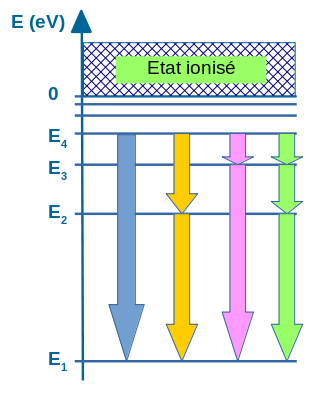
La désexcitation de l'atome étant une diminution d'énergie, l'atome doit "perdre" (ou plus précisement doit "émettre") de l'énergie.
Cela se fait par l'émission d'un photon.
2- Le photon :
Cette notion de photon (particule de lumière) avait été énoncée par A.Einstein en 1905 pour expliquer l'effet photoélectrique (extraction d'électrons de la matière par un faisceau de lumière). C'est d'ailleurs pour cette explication du phénomène qu'il a reçu le prix Nobel en 1921, alors que le grand public le connait davantage pour sa théorie de la relativité...
C'est avec le photon qu'est abordée la notion de dualité onde-corpuscule, notion qui sera étendue ensuite à toute la matière.
La lumière peut être perçue selon deux aspects distincts :
- comme une onde (exemple dans les expériences de diffraction ou d'interférences) qui est un phénomène continu
- comme constituée de "paquets" d'énergie, les photons (exemple : effet photoélectrique), phénomène discontinu
A une radiation lumineuse de fréquence ν (et de longueur d'onde λ ) , on peut associer un photon d'énergie :
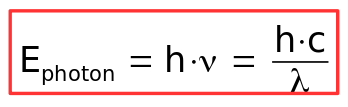

avec :
- h = 6,626.10-34 J.s-1 ; h est la constante de Planck (physicien ayant travaillé sur le rayonnement du corps noir)
- ν la fréquence de l'onde lumineuse (en hertz : Hz)
- λ la longueur d'onde de l'onde lumineuse (en mètre : m)
- c = 2,998.108 m.s-1, la célérité de la lumière dans le vide
3- Emission spontanée :
Lorsque l'atome est dans un état excité En , sa désexcitation le fait revenir dans un niveau d'énergie inférieure Ep , et ceci par émission d'un photon. Cette désexcitation est symbolisée par le diagramme suivant :
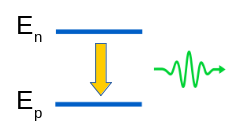
Le photon emporte la différence d'énergie En - Ep qui existe entre les deux niveaux concernés. On en déduit :
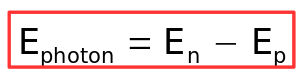
or
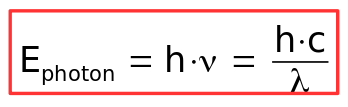
d'où :
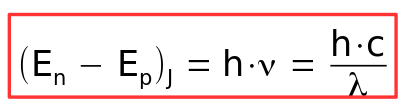
Remarque : dans cette expression (ci-dessus) toutes les grandeurs étant exprimées dans le système international d'unités, les énergies En comme Ep doivent être en joules (J). Or cette unité n'est pas bien adaptée au niveau microscopique, niveau pour lequel on préfère travailler en électron-volt (eV) avec :
1 eV = 1,6.10-19 J
On préfère alors utiliser cette relation dans laquelle le terme e (=1,6.10-19) sert de facteur de conversion en eV :
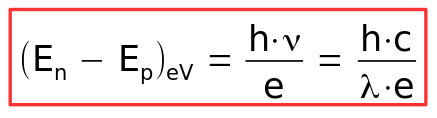
Il devient alors plus facile de travailler avec les diagrammes de niveaux d'énergie des atomes (donnés en eV)
Exercice : Niveaux d'énergie de l'atome d'hydrogène
1- Les différents niveaux d'énergie de l'atome d'hydrogène sont donnés en eV par la relation :
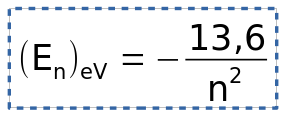
où n représente le nombre quantique principal c'est à dire ici le numéro du niveau électronique
- Calculer la valeur de chacun des 7 premiers niveaux de l'atome d'hydrogène (E1, E2, ..., E7)
- Les représenter sur un diagramme de niveaux d'énergie.
2- On suppose que l'atome d'hydrogène est dans le premier niveau excité. Il se désexcite en retombant sur le niveau fondamental. Calculer la longueur d'onde de l'onde électromagnétique associée au photon émis lors de cette désexcitation. A quel domaine du spectre électromagnétique appartient cette radiation ?
3- Aller sur le site : http://ostralo.net/3_animations/swf/spectres.swf et afficher le spectre d'émission de l'atome d'hydrogène (sélectionner dans le tableau des éléments le symbole de l'atome d'hydrogène et cocher la case "Raies de l'atome" uniquement) : on observe cinq raies d'émission dans le visible. (Cette série de raies est appelée série de Balmer)
La raie de couleur rouge est appelée la raie Hα ; c'est une raie importante en astronomie car l'hydrogène est un élément majeur dans l'univers.
- Mesurer à l'aide la souris la longueur d'onde λ de cette radiation
- Calculer l'énergie du photon associé
- Déterminer la transition électronique concernée par cette émission (il s'agit de déterminer entre quels niveaux d'énergie de l'atome d'hydrogène cette transition a eu lieu)
4- On suppose que l'atome d'hydrogène est dans le niveau excité E5 et qu'il retombe directement sur le niveau excité E2. Montrer que la radiation émise lors de cette transition correspond à l'une des radiations visibles dans ce spectre. Préciser laquelle.
C- Absorption de lumière par un atome :
C'est en quelque sorte le phénomène inverse de celui d'émission spontanée :
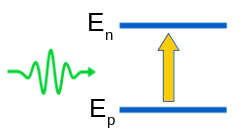
Lorsqu'un atome est dans un niveau d'énergie Ep (que ce soit le niveau fondamental ou un niveau excité), l'arrivée d'un photon sur cet atome pourra le faire passer dans un niveau d'énergie supérieur En à condition que ce photon ait EXACTEMENT l'énergie nécessaire pour faire passer l'atome de Ep à En : ni plus, ni moins.
Il faut donc que :
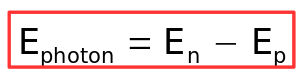
On retrouve alors la même relation entre les caractéristiques (ν , λ ) de l'onde lumineuse absorbée et les valeurs des niveaux d'énergie concernés par la transition :
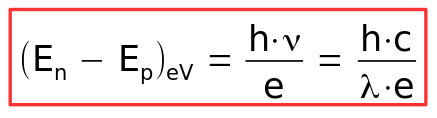
(on a redonné ici la relation en eV)

On déduit de tout cela deux propriétés importantes qui viennent confirmer un constat expérimental :
- un atome peut absorber les mêmes radiations que celles qu'il peut émettre. Le spectre d'émission et le spectre d'absorption d'un atome présentent donc des raies aux mêmes longueurs d'ondes :

- deux atomes diférents ont des structures électroniques différentes, donc des niveaux d'énergie différents. Les différents écarts (En - Ep) étant alors différents leurs spectres le sont également. Un spectre d'émission, comme un spectre d'absorption est donc en quelque sorte la "carte d'identité" de l'atome. Ce constat fait de la spectroscopie un moyen d'investigation scientifique très puissant car il permet même à distance l'analyse de la composition d'objets (exemple en astronomie)
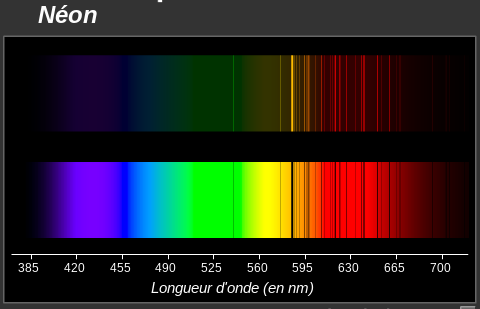
Le spectre du néon est différent de celui de l'hydrogène
Exercice : Niveaux d'énergie de l'atome d'hydrogène (suite)
5 - L'atome d'hydrogène étant dans son niveau fondamental :
- Peut-il absorber un photon d'énergie Ephoton = 9,0 eV ?
- Peut-il absorber un photon d'énergie Ephoton = 11,2 eV ?
- Peut-il absorber un photon d'énergie Ephoton = 12,09 eV ?
Si oui, préciser la transition électronique concernée par cette absorption.
6- L'atome d'hydrogène étant dans le niveau d'énergie E3, quelle serait la longueur d'onde de la radiation associée au photon qui serait capable de faire passer l'atome au niveau E4 ? A quel domaine spectral appartiendrait cette radiation ?
Emission stimulée : le Laser
II- Emission stimulée : le Laser
A- Deux sources de lumières très différentes :
Ci-dessous deux sources de lumière contenant toutes les deux un tube contenant des atomes de néon à l'état gazeux. Ces atomes sont excités ; la désexcitation entraîne dans chacun de ces tubes l'émission de photons donc de lumière. Pourtant le comportement est très différent :


sources : sonodis et jeulin
- A gauche : une lampe spectrale au néon émet de la lumière dans toutes les directions...
- alors qu'à droite un laser hélium-néon emet un faisceau très directionnel.
Pourquoi une telle différence de comportement ?
Deux animations du site https://phet.colorado.edu vont nous aider à comprendre.
1- Simulation d'une lampe spectrale :
Avant de visionner une séquence de cette animation, voici quelques explications sur les éléments qui la composent
- partie centrale : elle représente la lampe spectrale. C'est là où se trouve la zone d'interaction entre atome (représenté par un cercle gris numéroté (le numéro indiquant le niveau d'énergie dans lequel se trouve l'atome : 1 pour le niveau fondamental E1). Un curseur permet de régler la tension d'accélération des électrons donc l'énergie cinétique de l'électron au moment de l'impact :
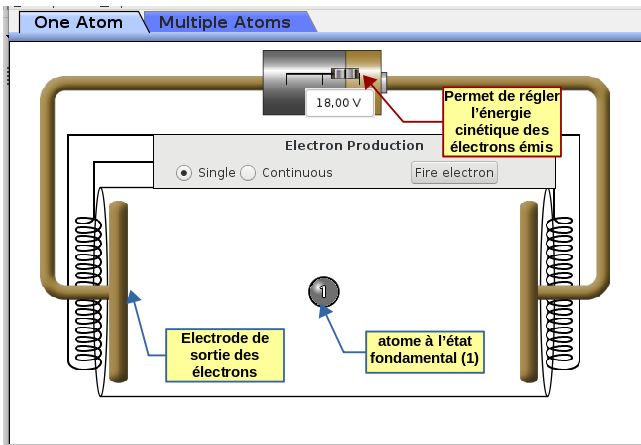
- Sur la partie droite de l'animation :
- Une légende explicative :
- bien repérer que l'électron est représenté sous la forme d'une sphère bien nette de couleur bleue, alors que le photon est représenté sous la forme d'une sphère diffuse pouvant prendre différentes couleurs (pas seulement celles indiquées ici)
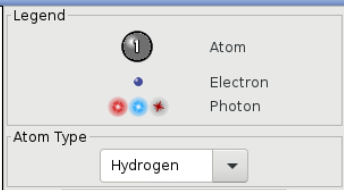
- on peut choisir le type d'atome qui se trouve dans la lampe spectrale : ici l'hydrogène
- la représentation des niveaux d'énergie de l'atome (E1 à E6) ainsi qu'une flèche rouge indiquant la valeur de l'énergie cinétique de l'électron incident au moment de la collision. Au cours de l'animation, on pourra voir les variations d'énergie de l'atome d'un niveau à un autre. On remarquera aussi que l'atome ne reste qu'un bref instant dans un état excité (dans la réalité, la "durée de vie" d'un niveau excité vaut ≈ 10-8s !).
- Une légende explicative :
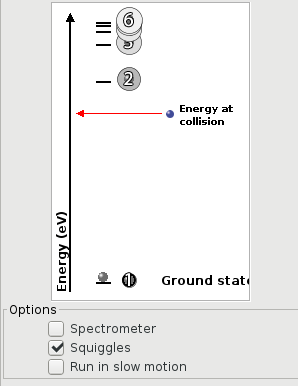
Dans cette première vidéo, on simule le choc entre un électron émis lors d'une décharge électrique et un atome d'hydrogène :
- première partie : l'énergie cinétique de l'électron est trop faible pour exciter l'atome de E1 à E2 : il ne se passe rien, l'électron continue son chemin
- deuxième partie : on augmente l'énergie cinétique Ec de l'électron pour qu'elle soit supérieure à E2. ATTENTION : il y a une différence notable entre l'absorption d'un photon (qui doit avoir exactement l'énergie requise, ni plus ni moins) et le choc entre un électron et un atome. L'électron n'est pas absorbé par l'atome : c'est l'énergie cinétique qui va l'être. L'atome va absorber l'énergie dont il a besoin (ici l'énergie pour passer de E1 à E2) et l'électron voit donc son énergie cinétique diminuée d'autant. L'électron laissant une partie de son énergie cinétique à l'atome, il ressort avec une vitesse moindre (ce qui n'est pas bien visible sur cette animation)
- troisième partie : on envoie sur cet atome d'hydrogène, en continu, des électrons d'énergie suffisante pour activer la transition E1 →E2 . L'atome émet alors à chaque fois un photon qui a toujours la même énergie (E2 - E1). Remarquer que la direction des photons émis est aléatoire :
Dans cette deuxièmevidéo, on a :
- réglé la tension d'accétlération des électrons à une valeur plus grande, dépassant le niveau E6
- ajouté un spectromètre cumulatif (chaque arrivée de photon est ajoutée sous la forme d'un carré coloré
En début de séquence on envoie les électrons au coup par coup pour voir le phénomène, puis on les envoie en continu pour accélérer la visualisation du résultat sur le spectromètre (dans le visible, mais aussi dans l'UV et l'infrarouge : remarquer la raie très importante dans l'UV (en gris à gauche) : c'est la retombée de E2 à E1 qui a lieu très souvent.
Une simulation un peu plus réaliste est réalisable en choisissant l'onglet "Multiple atoms" .
Dans cette simulation, on constate qu'une lampe à décharge va émettre une lumière polychromatique constituée de raies bien distinctes. Les photons émis le sont indépendamment les uns des autres et dans des directions quelconques :
Pour manipuler cette simulation par soi-même, il faut la télécharger (nécessite Java sur son PC) :
https://phet.colorado.edu/en/simulation/legacy/discharge-lamps
Une version directement en ligne (sans avoir à installer Java si on ne l'a pas) est disponible ici (mais elle est très lente) :
https://phet.colorado.edu/sims/cheerpj/discharge-lamps/latest/discharge-lamps.html
2- Simulation d'un Laser :
Avant d'aborder le principe de fonctionnement du Laser, il faut s'intéresser à un autre phénomène prévu par A.Einstein dès 1917 (environ 40 ans avant la réalisation des premiers Lasers) : l'émission stimulée.
Emission stimulée :
Lorsqu'un atome est dans un niveau excité En , l'arrivée d'un photon sur l'atome peut provoquer la désexcitation vers un niveau inférieur Ep, si ce photon a exactement l'énergie correspondant à la différence d'énergie En - Ep . La désexcitation de l'atome entraîne la formation d'un photon d'énergie En - Ep donc identique au photon incident
Le photon incident n'est pas absorbé.
Il ressort deux photons absolument identiques :
avant : après :
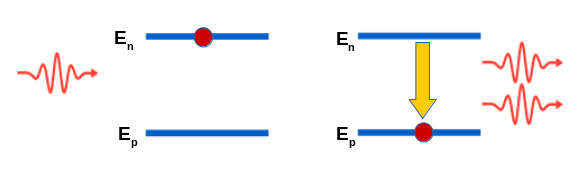
Les deux photons sortant ont la même énergie, sont en phase et ont la même direction.
Rque : le point rouge sur ce diagramme est là pour indiquer l'état dans lequel se trouve l'atome
On peut alors imaginer un dispositif dans lequel ces photons ayant ces propriétés bien particulières pourraient à leur tour être à l'origine d'autres émissions stimulées qui à leur tour etc... entraînant au final un important flux de photons :
- de même énergie ( = même longueur d'onde, donc une radiation lumineuse monochromatique)
- ayant tous entre eux une relation de phase
- ayant tous la même direction
Ce dispositif, c'est le LASER (Light Amplification by Stimulated Emission of Radiation)
Maximiser l'émission stimulée :
Pour que les deux photons identiques, émis en phase, puissent avoir la chance d'induire à leur tour des émissions stimulées, il faut qu'ils rencontrent des atomes excités sur le niveau En. Or on a évoqué que la durée de vie ("life time" en anglais) d'un état excité est très courte (de l'ordre de 10-8s), ce qui fait que si l'on regarde une grande population d'atomes, la très grande majorité est dans l'état fondamental. Nos deux photons vont quitter le dispositif sans avoir pu rencontrer d'atomes dans l'état excité.

Ci dessous, une situation "normale" :
un grand nombre d'atomes dans le niveau fondamental,
et quelques uns dans un état excité :
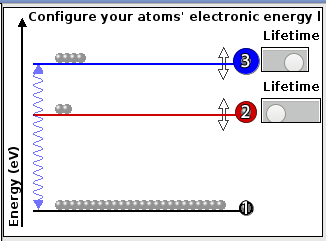
Pour augmenter la probabilité de rencontre photon ⇔ atome excité, il faut réussir à avoir un grand nombre d'atomes dans l'état excité, et donc réaliser ce que l'on appelle "l'inversion de population". Différentes techniques sont possibles pour faire cette inversion. Alfred Kastler (prix Nobel de Physique en 1966) l'a réalisé en premier à l'aide de lampes à décharge. Il a nommé cette technique "pompage optique".
Exemple d'une inversion de population :
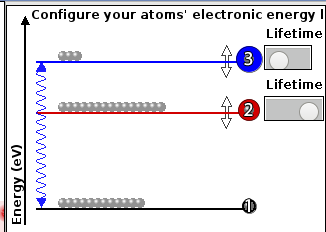
Simulation du Laser :
Commençons de nouveau par expliquer la simulation en légendant les nombreux éléments visibles :
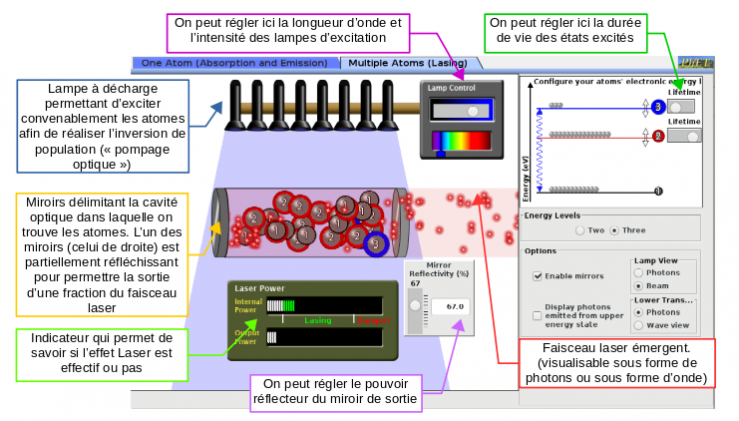
Trois niveaux d'énergie sont utilisés ici :
- les deux niveaux inférieurs (1 et 2) sont ceux pour lesquels l'inversion de population va être réalisée. C'est donc entre ces deux niveaux que se réalisera l'émission stimulée. La longueur d'onde du laser est celle associée aux photons ayant une énergie égale à la différence d'énergie entre ces deux niveaux.
- le niveau supérieur (3) : les atomes dans le niveau fondamental sont excités sur ce niveau supérieur (3) par les lampes à décharge. La desexcitation se fait sur le niveau (2). Pour obtenir l'inversion de population souhaitée, il faut que la durée de vie du niveau (3) soit inférieure à celle du niveau (2), ce qui permet. Sur l'animation cela se "règle". Dans la réalité c'est le choix judicieux des atomes et des transitions qui permettra la réalisation de tel ou tel type de laser !
Déroulé de l'animation :
- on commence par activer les lampes à décharge, ce qui permet d'exciter les atomes.
- pour avoir l'inversion de population, on rend la durée de vie de l'état excité (3) plus petite que celle de l'état excité (2)
- on commence à voir des photons appariés, mais ils sortent dans des directions quelconques
- pour avoir l'effet Laser, il faut les obliger à faire des aller-retours dans la cavité optique grâce à la présence de miroirs. L'un d'eux doit être partiellement réfléchissant.
- L'effet Laser a lieu. Le faisceau sortant pouvant être vu sous forme d'onde, on constate qu'en sortie on a une onde sinusoïdale pure (donc une seule fréquence, donc une seule longueur d'onde : on a donc une lumière monochromatique)
- L'énergie disponible dans le faisceau Laser provient de l'excitation des atomes, donc de la présence d'une source d'énergie extérieure : ici les lampes à décharge. En fin d'animation, on coupe les lampes à décharge : l'effet Laser disparaît.
Une bonne idée serait d'essayer par soi-même cette animation, il faut la télécharger ici (mais nécessite java pour fonctionner) :
https://phet.colorado.edu/en/simulation/lasers
On verra alors que ce n'est pas si simple d'avoir l'effet Laser : entre le Laser qui ne démarre pas et celui qui est en surchaffe !....
Le dispositif laser permet d'avoir un faisceau lumineux :
- monochromatique
- directif : il y a donc une concentration spatiale de l'énergie
Cette énergie peut être délivrée de façon continue (comme sur l'animation), mais aussi de façon pulsée ce qui permet de concentrer dans le temps l'énergie distribuée. On parle alors de concentration temporelle.
Toutes ces propriétés donnent au Laser une multitude d'applications dans des domaines très variés : industrie, médecine, recherche/enseignement, télécommunications, loisirs....
Remarque : grâce à ces propriétés, il est extrêmement facile de mettre en évidence en classe le phénomène d'interférences lumineuses : un laser , une double fente et un écran suffisent ! Pas de réglage à faire, et le résultat est visible à distance. Avec un dispositif du type "miroirs de Fresnel" présenté dans le lien ci-dessus, il faut parfois s'armer de patience avant d'arriver à voir ces fameuses interférences...
Applications du laser :
Un document du CEA :
Exercices :
- ChemCam : un laboratoire sur Mars
- Granulométrie d'une poudre (une application industrielle, ... et un retour sur la diffraction)
- Transmission laser (un petit retour sur le numérique...)
Domaines spectraux
Transitions d'énergie et domaines spectral :
1- Transition d'énergie électronique :
Comme cela a été évoqué dans les paragraphes précédents, les niveaux d'énergie atomiques correspondent aux niveaux électroniques.
Quand on regarde un diagramme de niveaux d'énergie pour un atome (ou pour un ion monoatomique), on constate que les valeurs sont de l'ordre de l'eV :
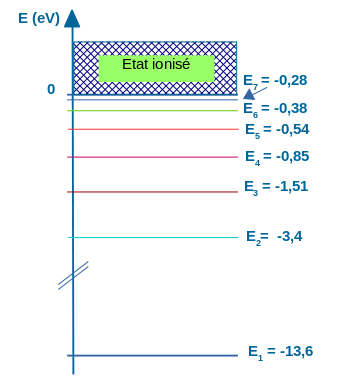

Les photons émis ou absorbés lors de transitions entre ces niveaux ont donc des énergies du même ordre de grandeur.
On peut alors calculer la longueur d'onde de l'onde électromagnétique associée à ces photons :
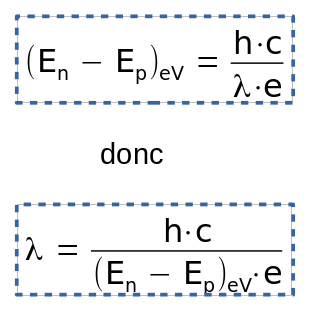
Dans cette relation, h, c et e sont des constantes. On peut calculer le rapport h.c / e et l'intégrer dedans, ce qui donne :

Pour une différence d'énergie :
- (En - Ep) = 10 eV on obtient λ = 124 nm ⇒ domaine de l'UV
- (En - Ep) = 1 eV on obtient λ = 1240 nm ⇒ domaine de l'IR
En prenant la relation dans un autre sens pour calculer la différence d'énergie en fonction de la longueur d'onde,
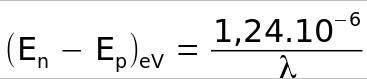
alors pour une longueur d'onde :
- λ = 400 nm on obtient (En - Ep) = 3,1 eV
- λ = 800 nm on obtient (En - Ep) = 1,55 eV
Un petit diagramme pour fixer les idées :
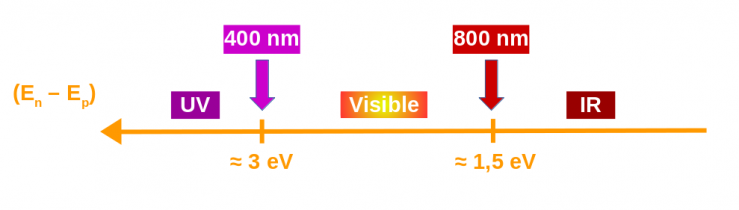
Tous ces résultats nous montrent que les spectres atomiques vont se développer essentiellement dans le visible et le proche UV ou le proche IR.
2- Transitions d'énergies vibratoires et rotationnelles :
Ces transitions d'énergie concernent les liaisons entre les atomes à l'intérieur des molécules (ou des ions poyatomiques).
Ces liaisons peuvent avoir des mouvements vibratoires ou de rotation :
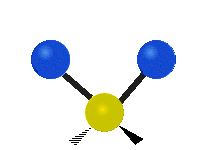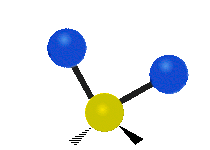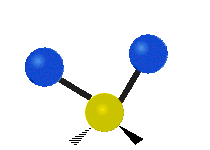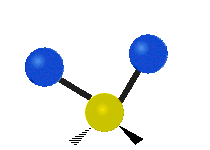
source : wikipédia
La réalisation de tels mouvements nécessitent de l'énergie. Typiquement, on a des énergies de l'ordre :
- du dixième d'eV pour les énergies vibrationnelles
- du millième d'eV pour les énergies rotationnelles.
On donne ci-dessous le spectre infra-rouge d'une molécule de formule brute C2H4O :
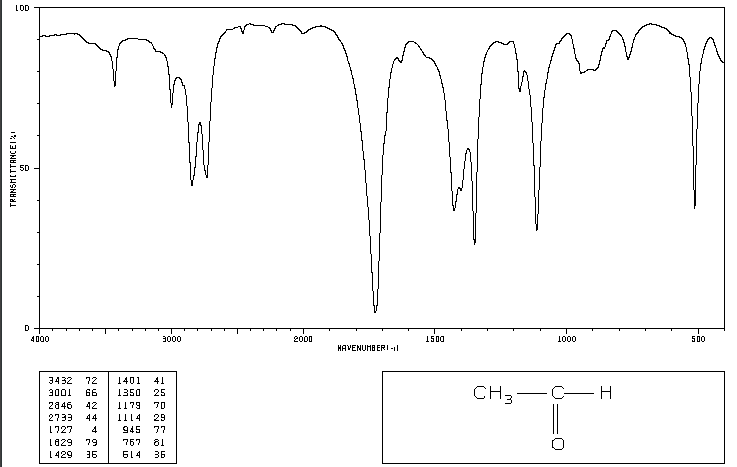
Source : Spectral Database for Organic Compounds
- Quel est le nom de cette molécule ?
- A quelle famille de composés organiques appartient-elle ?
- Sur ce spectre, le pic important à σ = 1727 cm-1 est dû à la liaison C=O. On rappelle que le nombre d'onde σ est égal à l'inverse de la longueur d'onde. Montrer que ce pic est dû à une transition d'énergie vibrationnelle pour cette liaison C=O (Attention aux unités)
3- Complément pour sa culture scientifique (hors programme TS Bac 2020) :
L'énergie du noyau est-elle aussi quantifiée : le noyau ne peut prendre que des valeurs d'énergie bien particulières. Il y a donc un état fondamental et des états excités. Les valeurs des niveaux d'énergie ne sont plus en eV mais en MeV (méga électron-volt) soit un million de fois plus élevées que pour les valeurs des niveaux d'énergie "électroniques" !
Suite à une désintégration, le noyau est profondément modifié puisqu'on change d'élément (Zfils différent de Zpère). Mais suite à ce changement, le noyau fils créé se retrouve non pas sur son niveau fondamental, mais sur un niveau excité.
A titre d'exemple voici le schéma de désintégration du cobalt 60 (source "Physique Nucléaire Appliquée" - F.Mayet - Editions De Boeck) :
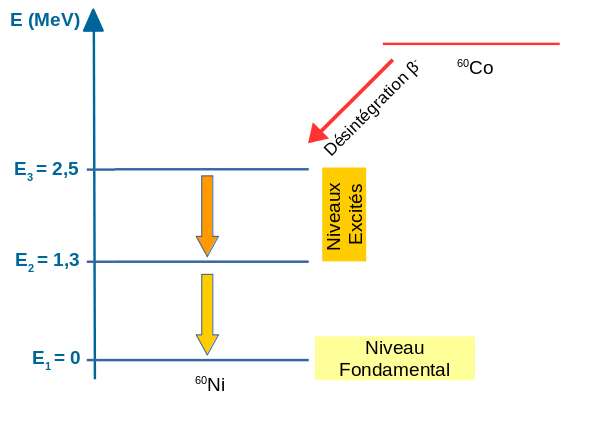
Le cobalt 60 est à un niveau d'énergie supérieur à celui du nickel 60. Il peut se désintégrer par voie β- ( = transformation d'un neutron du noyau en proton et émission d'un électron) selon la réaction :

Le noyau de nickel produit étant dans un état excité, il se desexcite par émission d'un photon :
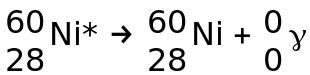
En fait la désexcitation se fait ici en deux étapes :
- transition E3 →E2 puis
- transition E2 → E1
→ Montrer que ces deux transitions aboutissent chacune à la formation d'un photon dont l'onde électromagnétique associée se trouve dans le domaine des rayonnements gamma du spectre (Voir ce lien pour les valeurs numériques)
Remarque : le danger du rayonnement gamma vient du fait que chaque photon embarque avec lui une énergie très importante (environ un million de fois plus importante que celle embarquée par un photon du visible !)