Cinétique chimique : éléments de cours
Introduction :
Vous avez déjà rencontré des transformations chimiques qui se font :
- quasi instantanément (par exemple l'explosion qui a lieu entre le dioxygène et le dihydrogène à l'approche d'une flamme ou d'une étincelle)
- sur des durées plus longues : on a le temps de voir évoluer par exemple un changement de couleur
- sur des durées extrêmement longues : on ne voit rien se faire si on reste quelques minutes devant mais c'est en revenant plusieurs jours ou semaines plus tard que l'on voit effectivement que le système chimique a changé : par exemple l'oxydation d'un morceau de fer dans l'air (= la rouille)
La cinétique chimique est là pour décrire et expliquer l'évolution d'un système chimique au cours du temps, et partant de là, voir comment on peut rendre une transformation plus rapide (intérêt économique pour l'industrie) ou au contraire plus lente (par exemple pour des raisons de sécurité). On évoquera alors les notions de facteurs cinétiques et la notion de catalyse et de catalyseurs.
Vision microscopique
Pour comprendre comment évolue une transformation chimique, il faut se plonger au niveau microscopique. C'est ce que permet l'animation décrite ci-dessous et disponible sur www.ostralo.net (elle nécessite le plugin flash pour fonctionner) :
Dans cette première fenêtre de présentation, on nous présente l'aspect graphique utilisé :
- le signe égal indique que la réaction pourrait se faire dans les deux sens (cas des réactions réversibles, mais dans une première approche on ne s'intéressera qu'à une réaction fonctionnant dans un seul sens écrite classiquement de la gauche vers la droite.
- Les réactifs seront donc pour nous les cercles bleus et rouges (appelons les pour la suite les molécules B ou R)
- Les produits seront les cercles verts et jaunes (appelés molécules V ou J)
Remarque : on utilise le terme de molécules mais cela pourrait être aussi des ions.
On entre ensuite sur la deuxième fenêtre pour paramétrer la simulation :
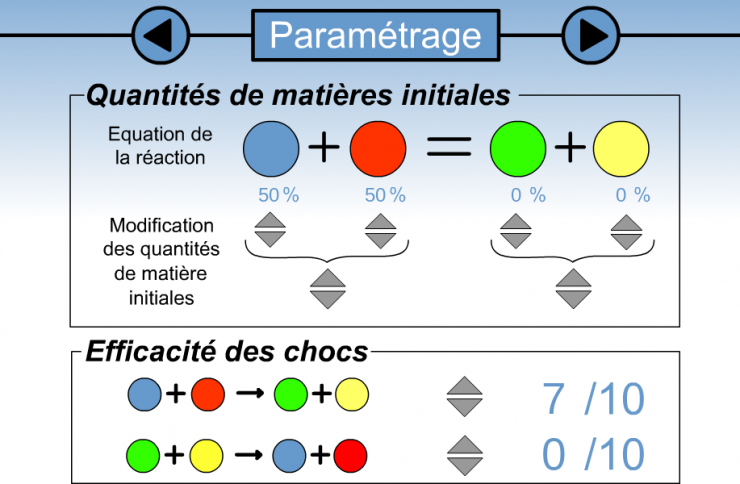
- Dans le premier cadre, on détermine la répartition des différentes espèces chimiques dans le système chimique initial. Par défaut, le système chimique est constitué de 50% de B, 50% de R et 0% de chacun des produits.
- Dans le deuxième cadre, vous allez découvrir ici une notion que vous ne connaissez pas encore : celle d'efficacité d'un choc entre deux réactifs.
C'est presque une évidence mais c'est ultra important pour comprendre la suite : pour que deux molécules puissent réagir, il faut qu'elles rentrent en contact !
Mais la réaction ne vas pas nécessairement se faire lors de ce choc et ce pour différentes raisons (la plus simple à comprendre porte sur la localisation des fonctions chimiques des deux molécules en interaction).
Par défaut, le logiciel a réglé la probabilité pour que le choc entre deux molécules B et R aboutissent à une réaction donnant V et J à la valeur de 7/10 soit 70%
La réaction inverse V + J donne B + R a été réglée à 0/10 soit 0%. Cela signifie que cette réaction ne peut pas se faire. (On sera donc dans le cas classique que vous connaissez bien : réaction dans le sens gauche droite uniquement)
Tous ces réglages sont modifiables (avec les flèches grises). Nous resterons ici avec le paramétrage par défaut.
Etape suivante : on nous montre le système chimique initial :
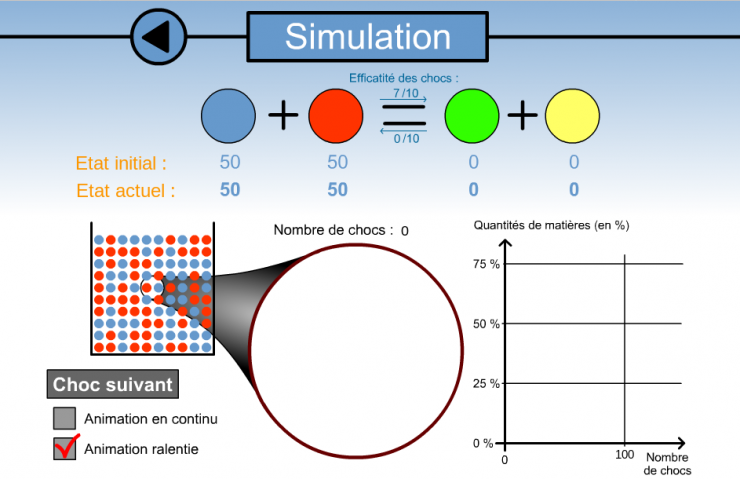
- La réaction est rappelée avec les efficacités choisies
- La ligne état initial nous rappelle que l'on a choisi 50 molécules B et 50 molécules R. On les retrouve mélangées aléatoirement dans le bécher.
- La ligne état actuel va évoluer au cours du temps : là elle est identique à la ligne 'Etat initial'
- Un zoom sur le centre du bécher est réalisé. Il permettra de bien visualiser les chocs entre molécules.
- Les quantités de molécules B restantes et de molécules V formées seront tracées au cours du temps dans le graphique à droite (R serait identique à B et J identique à V donc ils ne sont pas tracés)
- Pour réaliser l'animation, on pourra :
- la réaliser au cas par cas avec le bouton 'Choc suivant' (à faire au début pour voir et bien comprendre ce qui se passe pour différents types de chocs)
- ensuite pour aller plus vite on pourra cocher 'Animation continue'
- et enfin pour ne pas s'endormir devant son écran (...) décocher 'Animation ralentie'
Remarque : le mélange réactionnel est 'mélangé' par le logiciel entre deux 'chocs' consécutifs
L'idéal est d'aller faire fonctionner cette animation (qui nécessite le plugin flash), sinon observer la capture d'écran dans la vidéo ci-dessous.
Rque : la vidéo a été coupée : dans sa version initiale elle dure une vingtaine de minutes :
Lors du suivi cinétique par spectrophotométrie de la réaction :
H2O2 + 2H++ 2 I- → 2 H2O + I2
on a pu montré que l'avancement x à un instant quelconque est égal à la quantité de matière en diiode I2 formé
Après quelques calculs, on a pu ainsi passer de la courbe d'absorbance A = f(t) à la courbe d'avancement x = f(t) que voici :
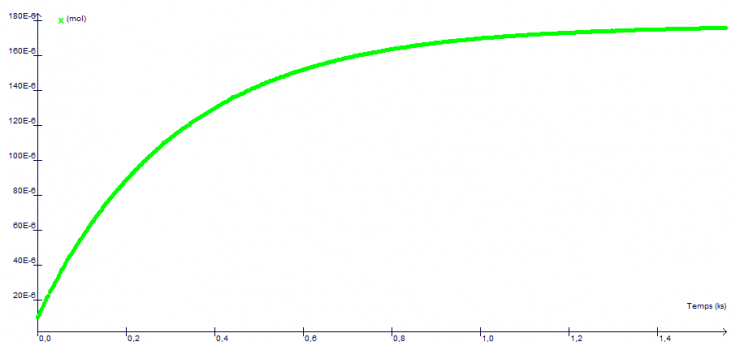
Cette courbe est très ressemblante dans sa forme à celle que l'on a eue dans la simulation pour la quantité de matière de l'espèce V produite :
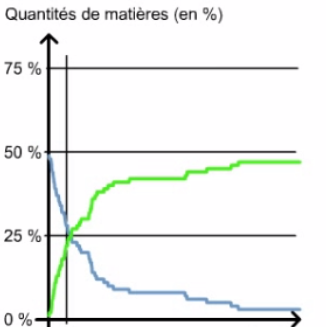
Rque : dans la simulation il n'y a que quelques dizaines de molécules en jeu ; dans une expérience réelle dans un bécher, ce sont des milliards de milliards de molécules qui sont présentes. L'effet statistique aléatoire est donc plus visible sur la simulation (aspect accidenté sur la courbe) que sur une mesure réelle (la courbe est 'lissée' par le grand nombre d'espèces présentes)
Interprétation microscopique :
Au départ, le système chimique ne contient que des molécules R et B : la probabilité pour qu'une molécule B et une molécule R se rencontrent est donc très grande :
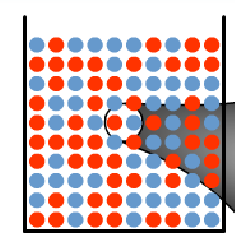
(Rque : la simulation ne 'regarde' que ce qui se passe 'au centre' du becher,
mais bien sûr les réactions se font dans tout le volume.)
Donc, après le mélange des réactifs, de nombreuses réactions R + B -> J + V se réalisent à chaque instant : le système chimique évolue à un rythme très rapide.
Mais ... de ces réactions résulte une diminution de R et B (remplacés par J et V) :
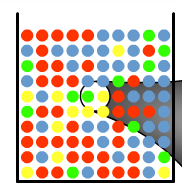
La conséquence : les molécules R et B ont donc de moins en moins de chances de se rencontrer et donc de réagir... et ce phénomène ne fait que continuer :
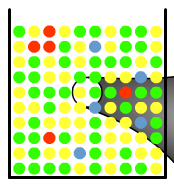
...ici les molécules R et B auront beaucoup moins de chances de se rencontrer.
Au fur et à mesure que la réaction avance, il faut de plus en plus de temps aux réactifs pour se rencontrer : le système chimique continue d'évoluer mais à un rythme plus faible
Conséquence au niveau macroscopique :
Reprenons la courbe x = f(t) tracée lors du TP et plaçons dessus quelques tangentes (notées 1 à 4) ci-dessous.
Rappel mathématique : la pente de la tangente donne la dérivée de la courbe en ce point ... et la dérivée donne de l'information sur la variation de la grandeur (ici l'avancement x)
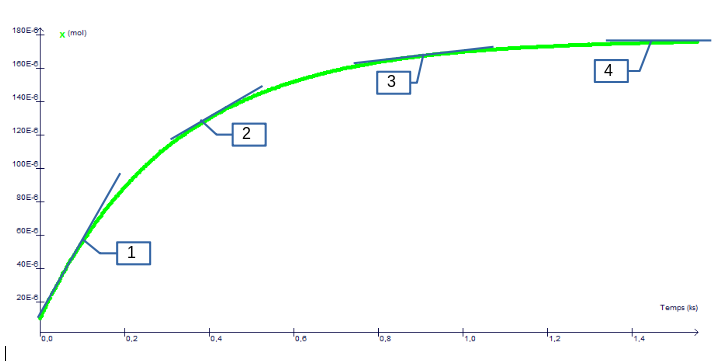
- La pente de la tangente est grande donc dx/dt l'est également : x varie de façon importante à chaque instant. La réaction 'avance' alors très vite. Par exemple, au niveau visuel (s'il y en a) les changements sont perceptibles.
- La pente de la tangente est plus faible : à chaque instant x continue d'augmenter mais de façon moindre. La réaction avance moins vite. Au niveau visuel les changements se font mais deviennent moins perceptibles
- Cela continue toujours dans le même sens
- La pente de la tangente est quasiment horizontale ... donc dx/dt tend vers 0 : la réaction n'avance quasiment plus. Dans le cas d'une transformation chimique dans laquelle un produit qui se forme est coloré (par exemple le diiode) alors la teinte ne semble plus évoluer. On dit que la réaction est 'finie', mais sans que l'on puisse donner un instant particulier à cette 'fin' de réaction.

et la façon dont l'avancement varie
( = confusion entre valeur de la variable et valeur de sa dérivée (par rapport au temps ici)) :
- à t = 0, l'avancement est nul ... mais sa dérivée est grande : cela signifie que juste après, x aura beaucoup changé !
- ensuite x ne fait qu'augmenter du début à la fin (où il atteindra sa valeur la plus grande !) tandis que sa dérivée dx/dt ne fait que diminuer (regarder la pente des tangentes 1 à 4 comment elle devient plus douce)
- à la 'fin' de la transformation chimique, x est à sa valeur maximum mais la valeur de sa dérivée est nulle
Temps de demi-réaction :

La mauvaise réponse : " Le temps de demi-réaction c'est la moitié du temps de réaction" ...
On a dit qu'il était impossible de déterminer un instant précis marquant la 'fin' de la réaction ... alors le diviser en deux ...
La bonne réponse : Le temps de demi-réaction c'est la durée nécessaire pour que l'avancement x atteigne la moitié de l'avancement final.
La démarche graphique :
- On détermine la valeur finale vers laquelle tend l'avancement : xf .
- On divise cette valeur par 2.
- On cherche à quel instant on a eu x = xf / 2.
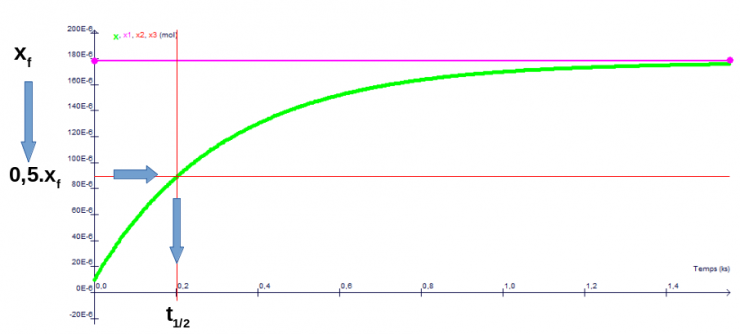
Attention : dans un tableau d'avancement, on demande souvent de calculer xmax (l'avancement maximum). Il ne faut pas confondre xmax et xf :
- parce que le rendement de la réaction n'atteint pas les 100 %, la valeur de l'avancement final n'ira pas jusqu'à la valeur xmax
- ou parce que la réaction est réversible (refaire une simulation en prenant une prenant une efficacité des chocs non nulle pour la réaction inverse J + V → R + B)
Facteurs cinétiques
Si on a compris le lien entre microscopique et macroscopique au niveau réactionnel, alors on doit pouvoir s'attaquer au problème suivant :
on dit que :
- la température à laquelle est porté le mélange réactionnel
- la concentration des réactifs (quand on est en phase liquide)
sont des "Facteurs cinétiques", c'est à dire qu'ils ont une influence sur la vitesse à laquelle se fait une réaction ( = ils modifient le temps de demi-réaction).
Dans quel sens ces facteurs cinétiques pourraient-ils jouer :
- Quel pourrait-être l'effet d'une augmentation de la température ou à l'inverse une diminution ? ( pour revoir cela il y a cette animation ou celle-ci )
- Quel pourrait être l'effet de l'augmentation ou de la diminution de la concentration de l'un des réactifs ?
Pour répondre à ces questions :
- penser microscopique (c'est quoi une augmentation de température au niveau microscopique ; c'est quoi une concentration plus grande : faire un petit schéma)
- est-ce que l'on a déjà rencontré l'effet de ces facteurs cinétiques dans la vie courante ? ...
1- Point de vue général :
Réaction chimique = rencontre entre réactifs
donc :
- pas de rencontre implique pas de réaction !
- la mobilité favorise les rencontres
- une grande quantité de réactif dans un petit volume favorise les rencontres
( transposé à l'épidémie de coronavirus, on retrouve ici les notions de mesure barrière et de confinement pour éviter la contamination individuelle et donc modifier considérablement ... la cinétique de l'épidémie ...)
2- Le facteur température
Augmenter la température du mélange réactionnel, c'est augmenter l'agitation de ses constituants donc leur mobilité.
- Une augmentation de la température permet donc d'augmenter la vitesse de réaction:
- en chimie on réalise souvent des transformations chimiques à des températures supérieures à la température ambiante. Par exemple au laboratoire, cela conduit à mettre en oeuvre des montages de type montage à reflux pour pouvoir augmenter la température du mélange réactionnel totu en limitant la perte de produits ou de réactifs par évaporation (c'est aussi une mesure d'hygyène et sécurité pour limiter la pollution de l'air du laboratoire)
- Pour diminuer la vitesse d'une réaction on plonge le mélange dans un bain d'eau glacée (voir la trempe de l'échantillon dans l'onglet 'suivi cinétique')
- ... à la maison on trouve :
- un autocuiseur qui permet de cuire plus vite les aliments ( dans une casserole la température de l'eau de cuisson reste au maximum autour de 100°C, mais dans l'autocuiseur qui est fermé, l'augmentation de la pression permet à l'eau de cuisson de monter à des températures plus élevées (un peu plus de 110°C) ce qui diminue la durée de cuisson
- un réfrigérateur : les aliments se dégradent (réactions chimiques telles que l'oxydation, mais aussi biochimiques). A température ambiante (20°C) ces réactions sont plus rapides que dans le réfrigérateur (4°C). On pourra donc conserver plus longtemps les aliments dans le réfrigérateur.
- un congélateur : là les températures très basses (-18°C) permettent de ralentir énormément toutes ces réactions de dégradation. Les aliments contenant beaucoup d'eau se retrouvent à l'état solide (donc il n'y a plus de mobilité). Les aliments congelés peuvent se conserver plusieurs semaines. Inconvénient : la structure peut être dégradée par le passage à l'été solide de l'eau contenue dans les cellules. Certains aliments supportent mal la congélation.

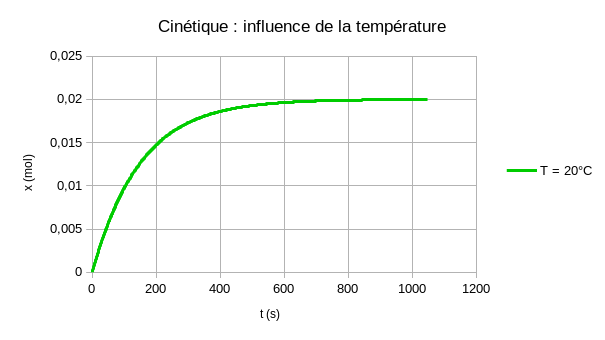
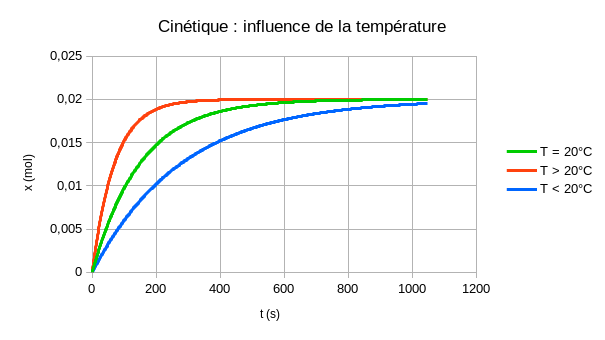
Comme le système chimique initial est le même, alors l'avancement final sera le même quelle que soit la température choisie.
Ainsi les courbes partent du même point (x = 0 à t = 0 s) et tendent asymptotiquement vers la même limite : xf.
A une température plus élevée, la vitesse de réaction est plus grande et la courbe se trouve donc toujours au dessus de celles relevées à températures plus faibles :
3- Le facteur concentration :
Prenons le cas d'une réaction dont l'équation serait :
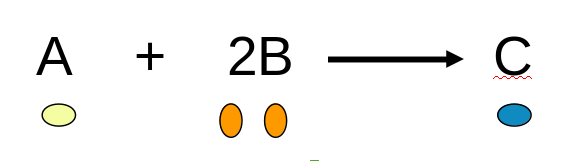
On va comparer deux mélanges réactionnels initiaux de même volume :
- Le mélange N°1 est stoechiométrique : il y a 6 molécules B pour 3 molécules A (le mélange des réactifs est bien dans les proportions de la réaction : 2 molécules de B pour 1 molécule de A. A et B vont donc disparaître et il se forme 3 molécules C
- Le mélange N°2 n'est pas stoechiométrique: il y a une proportion de molécules B trop importante : 11 molécules B pour 3 molécules A. Seulement 6 molécules B pourront réagir avec les 3 molécules A, ce qui donnera là aussi 3 molécules C. Il restera donc des molécules B (B est le réactif en excès) :
mélange N°1: mélange N°2 :
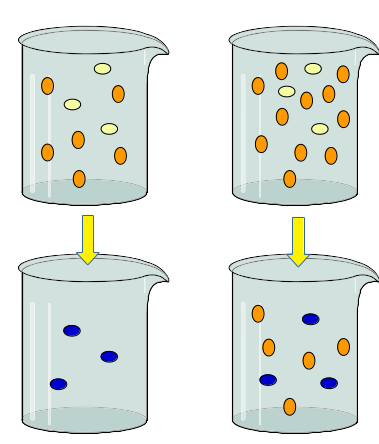
Dans le même volume, les molécules B sont plus nombreuses dans le mélange 2 que dans le mélange 1. Chaque molécule A aura donc davantage de chances de rencontrer des molécules B dans le mélange 2. La transformation chimique sera donc plus rapide dans ce mélange N°2.
Si pour un même volume de mélange réactionnel le bécher 2 contient plus de molécules B que le bécher 1, c'est donc que la concentration de B y est plus grande :
[B]2 > [B]1
On en déduit que la concentration est un facteur cinétique : augmenter la concentration de l'un des réactifs permet d'augmener la vitesse de réaction.
Remarques :
- On change la concentration d'un seul réactif (changer la concentration des deux impliquerait une plus grande quantité de matière des deux réactifs et donc un avancement final supérieur)
- En fin de réaction, il reste dans le mélange réactionnel un des réactifs en excès : il faudra être capable de séparer aisément le produit formé de cet excès de réactif (sinon l'intérết de l'augmentation de la vitesse de réaction pourrait être discutable)
- Une diminution de la concentration entraîne une diminution de la vitesse de réaction : c'est pour cela qu'intuitivement on rince (= dilution) abondamment une partie du corps accidentellement exposée à un produit chimique
- C'est ce facteur cinétique qui est responsable de l'infléchissement de la courbe x = f(t) au cours du temps :

- en 1 il y a beaucoup de réactifs dans le volume réactionnel : leur concentration est grande
- en 2, puis 3, puis 4, la quantité de réactifs a diminué mais le volume est resté le même : leur concentration a diminué et la vitesse de réaction (liée à dx/dt donc à la pente de la tangente) diminue.
4- Influence du solvant
Lorsque l'on a des réactifs en solution, le solvant utilisé aura un influence sur la cinétique de réaction.
Les ions ou molécules de soluté se retrouvent solvatées dans le solvant : des molécules de solvant viennent entourer en nombre plus ou moins grand les ions ou molécules de soluté :
ion sodium solvaté par des molécules d'eau :
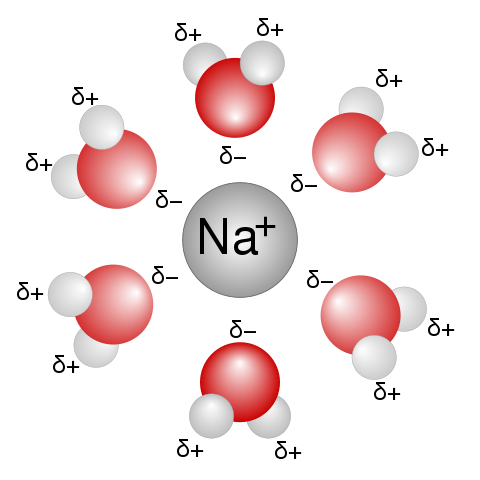
(source : wikipedia)
La présence de molécules de solvant autour de l'espèce solvatée modifie sa mobilité, et donc la cinétique de la réaction sera modifiée selon la nature du solvant
Suivi cinétique
Comment faire, pour explorer expérimentalement la cinétique d'une réaction ?
Le but est d'obtenir (en principe) le graphe représentant l'avancement de la réaction au cours du temps x = f(t).
Or le tableau d'avancement établit un lien entre quantité de matière (d'un réactif ou d'un produit) et avancement x.
Donc pour avoir x il faut avoir des mesures donnant une quantité de matière (d'un réactif ou d'un produit) :
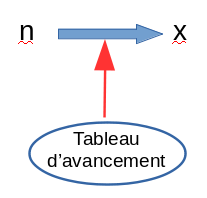
Comment avoir n ?
1- Mesure au cours du temps d'une grandeur physico-chimique :
Principe général :
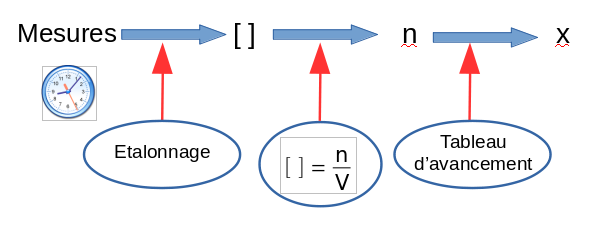
Exemple 1 : Suivi spectrophotométrique :
Dans le mélange réactionnel, l'un des produits qui se forme est coloré (toutes les autres espèces étant de préférence incolores). C'est le cas du TP étudié (formation du diiode).
On place un échantillon du mélange réactionnel dans le spectrophotomètre, et on vient lire sur l'écran, à instants réguliers, la valeur de l'absorbance. Ceci peut aussi se piloter par un PC :
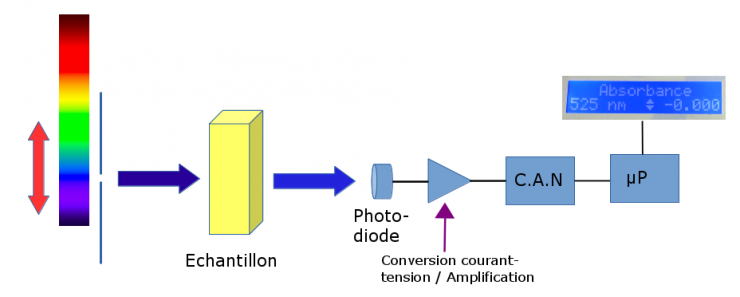
- On mesure au cours du temps l'absorbance A du mélange réactionnel
- On a un lien entre l'absorbance A et la concentration [ ] de l'espèce qui absorbe (par la loi de Beer Lambert), ce qui a nécessité la réalisation d'un étalonnage préalable
- A partir de la concentration, on peut obtenir la quantité de matière
- et de là, à l'aide du tableau d'avancement on récupére les valeurs de x pour les différents instants de mesure
Ce principe est applicable également lorsque l'on a un réactif coloré qui se transforme en un produit incolore. L'absorbance diminuera au cours du temps, mais après les différents calculs mis en place on verrait une courbe x = f(t) varier de façon croissante comme dans notre TP.
Exercices de type bac :
- Polynésie 2003 (un vieil exercice qui permet de revoir le principe du TP)
- Liban 2011 (parties B : 1 et 2 (pas la 3 qui porte sur la vitesse de réaction)
Exemple 2 : suivi conductimétrique :
La réaction a lieu :
- entre des réactifs ioniques et produit des molécules,
- ou à l'inverse les réactifs sont moléculaires et il se forme des ions.
On a donc une variation de la conductivité au cours du temps (en diminution, premier cas, ou en augmentation pour le second)
Le schéma de raisonnement sera le même que précédemment en remplaçant 'mesure d'absorbance' par 'conductivité' (bien sûr on travaillera avec un conductimètre et non plus au spectrophotomètre...) et loi de Beer-Lambert par loi de Kohlrausch :
- On mesure au cours du temps la conductivité du mélange réactionnel
- On a un lien entre la conductivité et la concentration [ ] de l'espèce qui absorbe (par la loi de Kohlrausch), ce qui a nécessité la réalisation d'un étalonnage préalable
- A partir de la concentration, on peut obtenir la quantité de matière
- et de là, à l'aide du tableau d'avancement on récupére les valeurs de x pour les différents instants de mesure
Exercice de type Bac sur cette technique (Bac S 2012 - Métropole) : un exercice de l'ancien programme (ne pas traiter la question 1.1)
Exemple 3 : suivi pressiométrique :
Dans le cas ou un produit formé l'est à l'état gazeux, il est possible de faire un suivi par mesure de pression à condition de ... confiner (désolé pour l'expression) ce gaz dans un récipient clos. La pression va alors monter au fur et à mesure que la réaction avance. Il faut bien sûr avoir tout bien prévu pour éviter une explosion ... Voici un document illustrant une telle manipulation que je faisais il y a quelques années. Parfois le bouchon sautait avant la fin de la manip... Des résultats de mesure se trouvent en dernière page du document : on y voit une courbe x = f(t) qui a quasiment la même forme que celles que l'on a pu rencontrer (sauf au tout début, car tout le comprimé ne s'est pas encore délité dans la solution).
2- Suivi cinétique par CCM
CCM : chromatographie sur couche mince (on pourra revoir le principe de la CCM dans cette animation)
Le principe de cette méthode de suivi cinétique est décrit dans le livre de chimie Belin TS 2012, notamment dans l'exercice 5 page 69 :

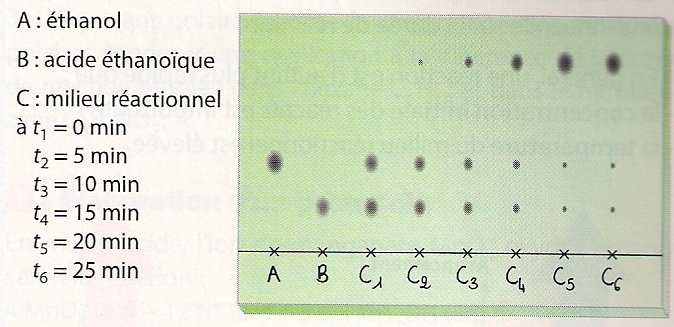
Cet exercice s'intéresse au suivi cinétique par CCM (voir image ci-dessus) d'une réaction d'esterification entre l'éthanol et l'acide éthanoïque.
Répondre aux questions de cet exercice
Voir également l'exercice "Suivi de réaction par CCM" page 257
3- Dosages d'échantillons
On prélève à des instants particuliers t un petit volume du mélange réactionnel et on l'analyse par un dosage direct. Le résultat du dosage permet de remonter par calcul à la valeur qu'avait l'avancement x à l'instant t du prélèvement.
Pour cela il faut néanmoins prendre la précaution suivante : on 'fige' l'état chimique de l'échantillon en le plongeant dans un bain d'eau glacée : la baisse rapide de la température ralentit alors énormément la réaction, ce qui l'empêche 'd'avancer' entre le prélèvement de l'échantillon à l'instant t et son dosage quelques dizaines de secondes plus tard. Cette technique s'appelle la trempe de l'échantillon. (Elle est basée sur le facteur cinétique température !)
Catalyse
1- Réaction de dismutation du peroxyde d'hydrogène H2O2
H2O2 intervient dans deux couples oxydant / réducteur : H2O2 / H2O et O2 / H2O2
Deux molécules de peroxyde d'hydrogène peuvent réagir entre elles pour donner de l'eau et du dioxygène.
→écrire les équations électroniques relatives à chacun des couples cités
→Vérifier que l'équation-bilan de la tranformation chimique est :
H2O2 + H2O2 →H2O + O2
Cette transformation chimique est extrêmement lente : des flacons d' eau oxygénée (nom commun du peroxyde d'hydrogène) se conservent très longtemps.
L'image ci-dessous extraite de cette vidéo, montre 3 béchers :
- au centre un bécher contenant de l'eau oxygénée : il ne s'y passe rien
- à droite un même bécher dans lequel on a ajouté un peu de chlorure de fer(III)
- à gauche un même bécher dans lequel est plongé un petit disque de plastique recouvert d'une fine pellicule de platine (un métal rare et cher) : c'est un dispositif qui sert à nettoyer les lentilles de contact
En présence de platine ou d'ions fer(III), la dismutation du peroxyde d'hydrogène devient rapide. A la fin de la transformation, le platine comme les ions fer(III) se retrouvent intacts dans le mélange réactionnels.
On dit que le platine; de même que les ions fer(III) sont des catalyseurs de la dismutation du peroxyde d'hydrogène.
2- Catalyse(s) et catalyseurs
Un catalyseur est une espèce chimique qui permet d'accélérer une transformation chimique mais qui ne rentre pas dans l'équation-bilan globale de cette transformation.
Cependant, un catalyseur agit au niveau du mécanisme réactionnel.
Exemple : la dismutation du peroxyde d'hydrogène en présence des ions fer(III) est remplacée par deux réactions chimiques successives, rapides, dont le bilan global est identique à celui de la dismutation.

- ne pas confondre facteur cinétique et catalyseur
- ne pas dire par exemple "le platine est un catalyseur" mais "le platine est un catalyseur de la réaction de dismutation du peroxyde d'hydrogène" (en effet une espèce chimique n'a pas la propriété de pouvoir catalyser toutes les réactions chimiques : être un catalyseur n'est pas une propriété intrinsèque mais une propriété spécifique à une situation donnée)
- dans la vie courante le terme catalyseur est utilisé à tort pour signifier "déclencheur" : le catalyseur ne déclenche pas une transformation chimique : il rend plus rapide une transformation chimique qui est thermodynamiquement possible.
Dans cette vidéo on voit deux cas de catalyse :
- Catalyse homogène : catalyseurs et réactifs sont dans une même phase (exemple du becher de droite). La cinétique dépendra alors de la concentration du catalyseur
- catalyse hétérogène : catalyseur et réactifs sont dans des phases différentes :
- cas du bécher de gauche (réactif en phse liquide, catalyseur en phase solide)
- pot catalytique sur les véhicules : (réactifs gazeux (les gaz d'échappement) , catalyseur solide)
Lorsque le catalyseur est solide, la cinétique de la catalyse dépend de la surface de contact entre le catalyseur et les réactifs : plus cette surface est grande et plus la catalyse sera efficace. On utilise donc ces catalyseurs sous forme divisée (poudres, granulés) ou sous forme alvéolaire (voir photo page 67)
Le produit d'une tranformation chimique peut être différent selon la nature du catalyseur : on dit qu'un catalyseur est sélectif
Catalyse enzymatique : lire le paragraphe 3.3 page 67
exemple : si on met de l'eau oxygénée sur une coupure un dégagement gazeux se produit (la dismutation du peroxyde d'hydrogène est catalysée par une enzyme se trouvant dans le sang : la catalase)
Résumé